涉及220个药品!一省公布新药和过评药品清单
发布时间:2024-07-19 11:49:26 阅读量:406
作者:医药健康资讯 来源:医药健康资讯
核心提示:近日,湖南省公共资源交易中心发布《关于新药和过评药品申报资料(2024年7月)核验结果的公示》。
近日,湖南省公共资源交易中心发布《关于新药和过评药品申报资料(2024年7月)核验结果的公示》。
根据梳理,公示的药品信息如下:
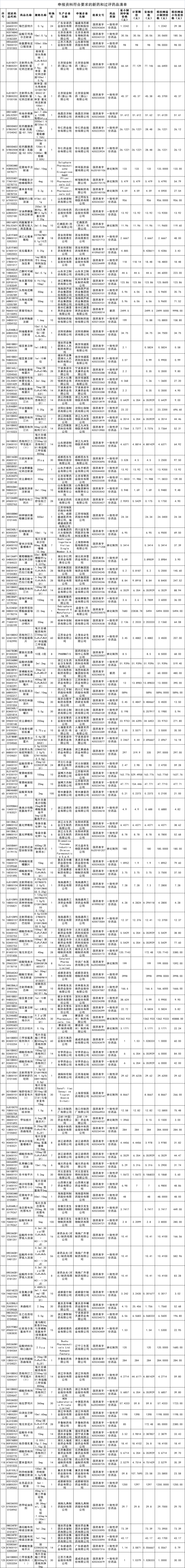
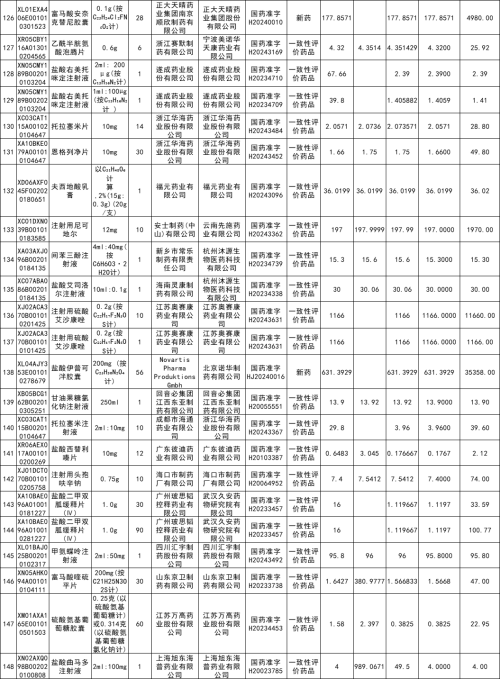
一、148个申报资料符合要求的新药和过评药品,涉及磷酸西格列汀片等110个品种和太极集团四川太极制药有限公司等98家生产企业、辉瑞制药有限公司等96家申报企业。(详见附件1)
湖南省公共资源交易中心完成了企业2024年7月1日至10日提交的新药及通过仿制药质量和疗效一致性评价类药品的申报资料核验,且经湖南省医保局复核。现将符合新药和过评药品申报要求的药品予以公示,公示期为2024年7月15日至20日。
如无异议的,公示期内,企业须登录湖南省药品和医用耗材招采管理子系统(以下简称“招采子系统”)的"药品招标管理"模块,在"价格联动管理"找到对应产品进行价格确认,确认的产品将纳入湖南省挂网药品目录,并标识为“新药”、“参比制剂”或“过评药品”,供医疗机构采购并执行新的挂网价格;公示期内企业未确认的产品暂不纳入湖南省挂网目录,可在下一申报周期重新申报。
如有异议的,企业应于7月20日17:00前,登录招采子系统,通过“申投诉管理”模块进行申投诉,逾期不予受理。申投诉的产品暂不纳入挂网药品目录,经省医保局复核后,届时按处理意见处理。
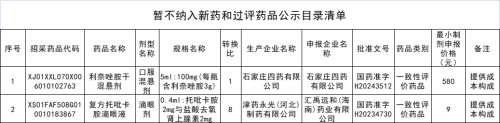
二、2个因拟挂网价格过高,暂不纳入公示目录的产品,具体包括:石家庄四药有限公司申报的利奈唑胺干混悬剂、汇禹远和(海南)药业有限公司申报的复方托吡卡胺滴眼液。(详见附件2)
上述2家企业需按照要求填报《药品价格信息表》,待医保局核定挂网限价后再按相关政策处理。(点击“阅读原文”查看)
三、68个因申报资料不全或资质不符合要求等原因审核未通过的产品,涉及法莫替丁注射液等55个品种和石家庄以岭药业股份有限公司等53家生产企业。(详见附件4)
上述产品可在下一申报周期补充资料后重新申报。
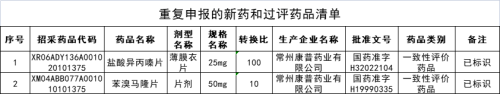
四、2个因重复申报视为无效申请,暂不予受理的产品,具体包括:常州康普药业有限公司的盐酸异丙嗪片和苯溴马隆片。(详见附件5)
附件1.申报资料符合要求的新药和过评药品清单
附件2.暂不纳入新药和过评药品公示目录清单
附件4.申报资料核验未通过的新药和过评药品清单
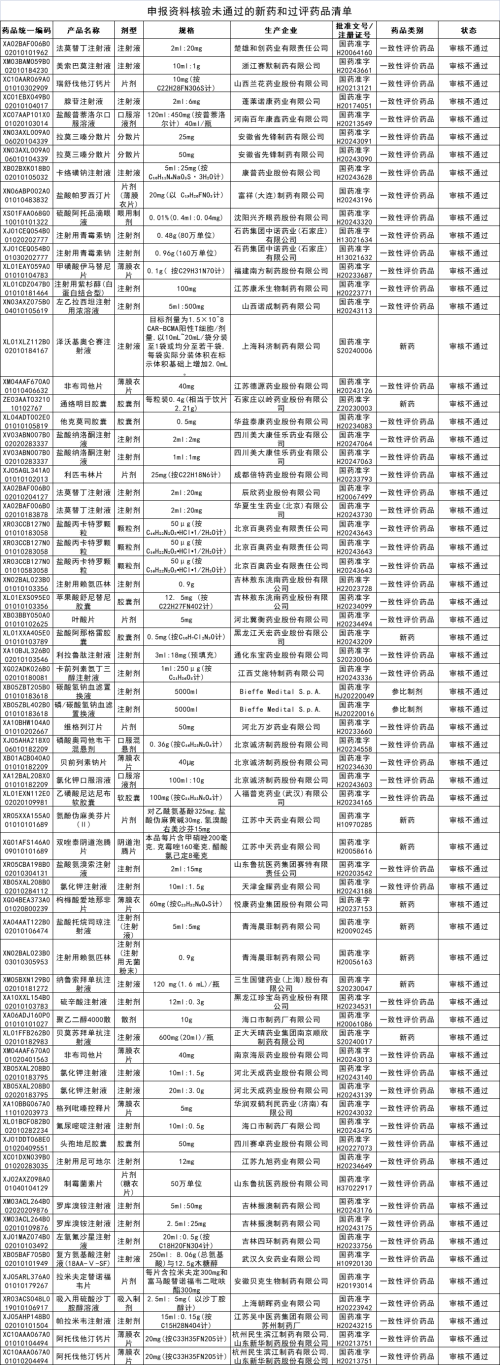
附件5.重复申报的新药和过评药品清单