涉141个产品、4个标识为红色!一省公示药价审核结果
发布时间:2025-02-06 17:50:12 阅读量:1174
作者:医药健康资讯 来源:医药健康资讯
核心提示:近日,广东省药品交易中心发布《关于转发<关于公示部分新增报名挂网药品价格审核结果的通知(20250126批次)>的通知》(下称《通知》),公示时间自本通知发布之日起至2025年2月6日24:00。
近日,广东省药品交易中心发布《关于转发<关于公示部分新增报名挂网药品价格审核结果的通知(20250126批次)>的通知》(下称《通知》),公示时间自本通知发布之日起至2025年2月6日24:00。
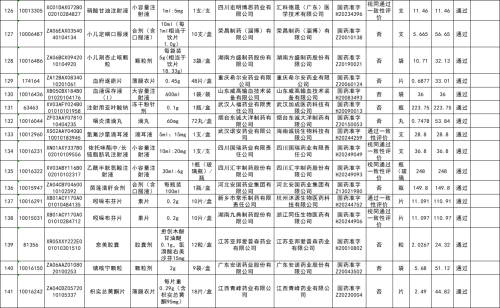
根据梳理,《通知》公示了141个已通过信息及分类审核且已申报价格的新增报名挂网药品,涉及胰酶肠溶片、强力天麻杜仲丸等117个品种和国药一心制药有限公司等105家生产企业。附表显示,这141个药品价格审核结果均为“审核通过”。(详见附件)
值得注意的是,武陟维尔康生化制药有限公司生产的胰酶肠溶片、河北凯威制药有限责任公司生产的溴米那普鲁卡因注射液和山西华卫药业有限公司生产的红花注射液,附表显示这3个产品无监测价,申报挂网价格仍明显高于同通用名其他厂牌药品挂网价格;此外,Patheon Italia S.p.A生产的艾加莫德α注射液(皮下注射),附表显示该产品无监测价,申报挂网价格仍明显高于同厂牌同剂型药品挂网价格。
《通知》指出,上述4个产品将标识为红色,当医疗机构下订单时提示价格风险“该产品明显高于同厂牌同剂型药品挂网价,请考虑是否继续采购。”
《通知》要求相关企业使用CA证书登录新招采子系统(以下简称子系统),通过“药品招标管理-药品挂网申报-公示信息”查看相关药品审核通过情况,并于公示期内完成《省级医药集中采购平台挂网申请表》的生成、签署及提交。
同时,《通知》指出,如对公示结果有异议的,请相关企业在公示截止时间前使用CA证书登录招采子系统,通过“药品集中采购管理-药品挂网申报-申投诉”进行反馈,点击“新增”后根据反馈内容在“申诉类型”选择“价格信息申投诉”,并按系统要求填写相关内容;如有附件应加盖单位公章。同一产品所涉及信息反馈,在子系统提交一次即可。未按要求递交信息反馈或逾期递交的,将不予受理。
附件.部分新增报名挂网药品价格审核结果公示表(20250126批次)